INDEX
【利益相反監理の流れ】
(1)利益相反の手続き
(2)利益相反確認のフロー
(3)利益相反管理
利益相反管理の流れ
(1)利益相反の手続き
研究を開始する前や研究者の追加の前、定期報告の際に、利益相反状況の確認が必要となります。一般的な確認手続きは「(2)利益相反確認のフロー」及び以下の参考資料をご覧ください。
【参考】
・臨床研究法における臨床研究の利益相反管理について(厚生労働省医政局研究開発振興課長通知)
・臨床研究法における利益相反管理ガイダンスに関する Q&A ver.1.0
・利益相反管理の手引き
(AMED 中央治験審査委員会・中央倫理審査委員会基盤事業
臨床研究法の統一書式及び利益相反様式の見直しについての検討WG 成果物)
東北大学内の研究者の手続き
- 申請方法はこちらをご覧ください。
- 利益相反に関する相談は「東北大学 法務室(利益相反マネジメント担当)」へご連絡ください。
学外の研究者の手続き
- 各施設で行う利益相反状況の確認方法については施設の手順により異なる場合がありますので、各施設の担当部門にご確認の上お手続きください。
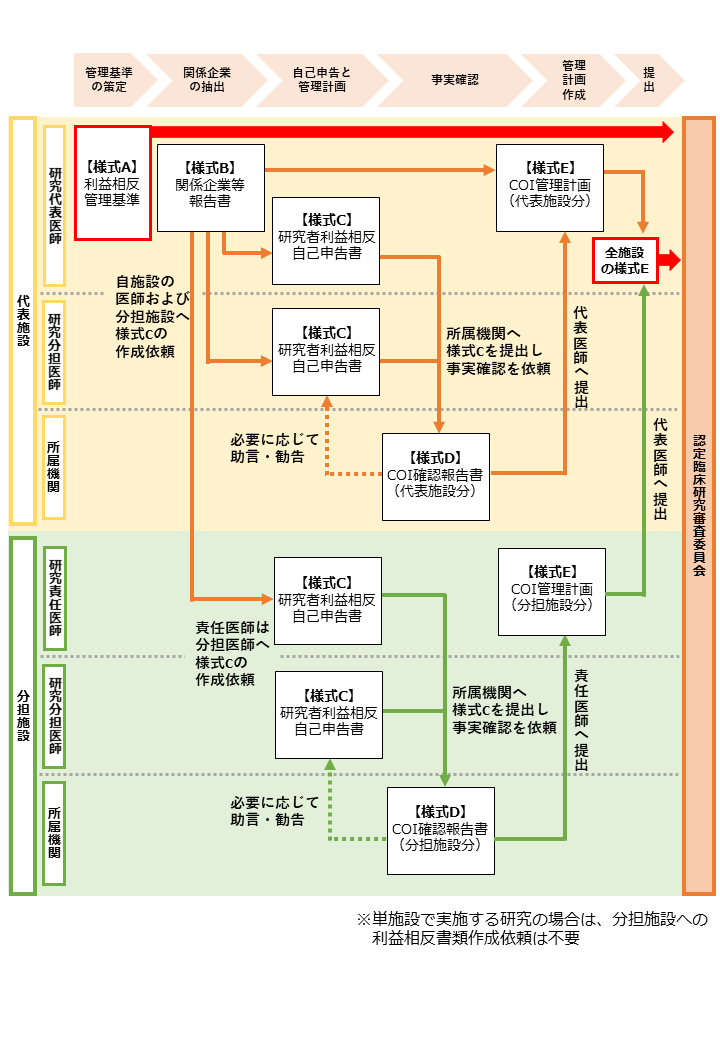
(2)利益相反確認のフロー
一般的な確認の流れは以下のとおりです。